Nowe strategie w chorobie Parkinsona
Z tego artykułu dowiesz się o:
• Terapii komórkami macierzystymi, immunoterapii, immunomodulacji według dr Simon’a Stott’a (Video)
Simon Stott jest zastępcą dyrektora ds. badań w organizacji The Cure Parkinson’s Trust. Przyjechał do Wielkiej Brytanii z Nowej Zelandii, po drodze spędzając kilka lat na pracy badawczej w Szwecji. W Anglii pracował z profesorem Roger’em Barker’em[1] w Cambridge, wtedy to także zaczął prowadzić bloga The Science of Parkinson’s gdzie prostą angielszczyzną tłumaczy meandry choroby Parkinsona (ChP). Na początku swojej prelekcji Stott podkreśla, że dokładne mechanizmy ChP nadal nie są znane, tym niemniej sporo się dzieje na poziomie badań klinicznych. We wspomnianym filmie zarysowuje on główne strategie walki z chorobą, które opiszę dla tych z Państwa co wolą czytać po polsku niż słuchać po angielsku. Stott pod koniec swojego wystąpienie umieścił podsumowanie, którym się posłużyłem, aby czytelniej zorganizować ten wpis. Oto nakreślone przez niego strategie opatrzone krótkim opisem
Terapia komórkami macierzystymi

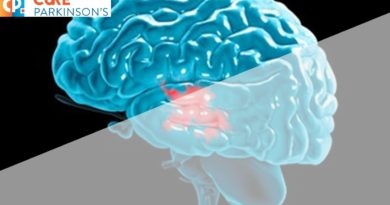
Rys.1. Putamen zaznaczony na czerwono
Źródło: Wikipedia
Strategia ta polega na wszczepianiu w miejsca ubytku w skorupie[2] (łac. putamen) (Rysunek 1) komórek pobranych z usuniętych płodów, które z czasem rozwiną się w neurony dopaminergiczne. Taka interwencja może skutkować fizyczną poprawą stanu zdrowia. Jednak ostatnio odkryto, że te wszczepione w latach 90-tych zdążyły w dość krótkim czasie nabrać cech typowych dla choroby Parkinsona, czyli tzw. cech patognomicznych. Zauważono bowiem, że zawierają one ciała Lewy’ego, czyli skupisk białeka, przede wszystkim alfa-synukleiny, i w konsekwencji tych wyników ukuto hipotezę rozprzestrzeniania się ChP na zasadzie choroby prionowej. Zgodnie z tą zasadą jedna toksycznie sformowana komórka potrafi wymusić na innych, zdrowych sąsiadach, taką samą patologiczną zmianę. Jednym z rozwiązań tego problemu może być immunoterapia a dokładniej wzmocnienie czy też może wyczulenie systemu odpowiedzi immunologicznej.
Immunoterapia
Wiele firm farmaceutycznych pracuję nad takimi szczepionkami. Dwie wiodące to znany gigant farmaceutyczny firma Roche, która w tym celu nawiązała współpracę ze zdecydowanie mniejszą firmą biotechnologiczną Prothena. Ich projekt badawczy, PASADENA PRX-002 będący w fazie drugiej badań klinicznych[3], czyli w fazie, gdzie bada się skuteczność i skutki uboczne został zakończony. Brało w nim udział 300 ochotników z ChP, których przez rok, co miesiąc, poddawano infuzji zawierającej przeciwciała. Terapia ta miała na celu definitywnie rozwiązać problem agregującej się alfa-synukleiny. Raport badań PASADENA’y ukazał się w grudniu 2020 (NCT03100149) zaś na stronie Michael’a J. Fox’a czytamy: Pomimo, że project PASADENA nie osiągnął głównego celu, odnotowano poprawę stanu zdrowia uczestników widoczną w wielu testach.
Inny projekt, BIIB054 nazwany Spark prowadzony przez firmę Biogen również jest w drugiej fazie i zaangażowanych weń jest trochę ponad 300 ochotników a wyniki ukażą się pod koniec roku 2022. Warto zaznaczyć, że jeśli chodzi o projekty immunologiczne to istnieje na tym polu silna konkurencja, oto inne podobne projekty: Medi341, ACI-870, Lu AF82422, BAN0805, PD1601, PD1602, UB-31.
To jednak nie wszystko, bo oprócz pasywnej szczepionki, prowadzone są prace nad opcją aktywnego szczepienia. Aktywna immunizacja, w przeciwieństwie do wersji pasywnej, polega na tym, że nasz system odpornościowy dzięki szczepionce sam uczy się tworzyć przeciwciała w tym wypadku zapobiegające koncentracji alfa-synukleiny [1]. Na wersji aktywnej skupia się Austriacka firma Affiris, która ogłosiła w tym roku, że jest gotowa rozpocząć fazę drugą, nie zdradzając jednak przy tym szczegółów projektu [link do artykułu-ang.]. Wiemy, że fazę pierwszą projektu określono jako sukces stwierdzając, że po czterech latach od szczepienia żaden ze 100 uczestników nie zgłosił wystąpienia skutków ubocznych.
Wszystkie te pozytywne wiadomości może ostudzić fakt, że podobne szczepionki testowane w kierunku choroby Alzheimera okazały się nieskuteczne. Rodzi się zatem pytanie czy ten sam los podzielą szczepionki na ChP?
Spekuluje się, że przyczyną niepowodzenia może być niewystarczająca koncentracja przeciwciał w ośrodkowym układzie nerwowym (OUN, lub z ang. CNS), na który składa się mózg i rdzeń przedłużony. Tutaj z pomocą przychodzi firma Enterin ze swoim projektem ENT-01 produkując substancje podobną do protein wytwarzanych przez kolenia pospolitego – odmiany rekina. Substancję znaną jako sqalamina (Amisterol), która oprócz tego, że posiada właściwości przeciwbakteryjne to potrafi także zapobiegać grupowaniu się alfa-synukleiny oraz tłumić toksyczne mechanizmy z tą agregacją związane. Ponieważ squalamina nie może przejść przez barierę krew-mózg służy jako lek w zaparciach [2] [3]. Co może być bardziej znaczące to to, że prowadzone są też badania nad jej siostrzaną wersją Trodusquemine’a, która ma właściwości penetracji do OUN. Co ciekawe nie zmniejsza ona rozmiaru skupisk owych źle złożonych białek, ale odsuwa je od komórek i w ten sposób zmniejsza ich toksyczny wpływ [4].
Należy też dodać, że inna firma Proclara biosciences – NPT189. prowadzi ciekawe badanie nad lekiem, który ma za zadanie hamować powstawanie wszelkich patologicznych skupisk (agregacji) co daje znacznie szersze zastosowanie (Rysunek 2)
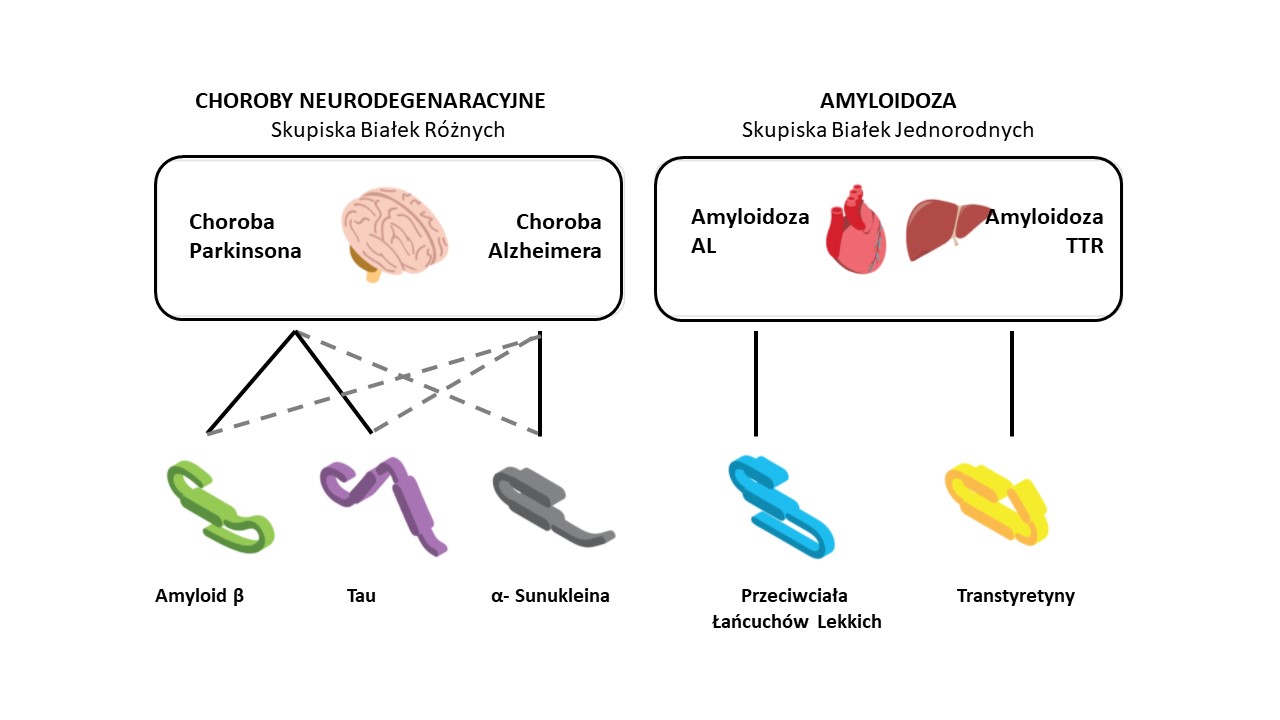
Immunomodulacja
Czyli strategia, gdzie zamiast wzmacniać system immunologiczny powściąga się go trochę. Podejście oparte jest m.in. na spostrzeżeniu, że osoby o osłabionym systemie immunologicznym rzadziej zapadają na ChP [5]. Zgodnie z inną hipotezą umierające neurony alarmują system immunologiczny, w tym komórki mikrogleji, które nie tylko oczyszczają nasz układ nerwowy z umierających neuronów, ale także stymulują produkcję dodatkowej alfa-synukleiny poprzez wysyłanie cytokinez, prozapalnych protein. Tak więc system immunologiczny jednocześnie czyszcząc przyczynia się do powstawania stanów zapalnych. Oto jak w skrócie rysuje się mechanizm ciągłego stanu zapalnego, który zdaję się działać na zasadzie błędnego koła.
Sargramostim
Lek, który jest już po pierwszej skromnej próbie klinicznej, ma w domyśle wyhamować ten proces. W fazie pierwszej brało udział 20 osób przez 12 tygodni co udowodniło dobrą tolerancje i bezpieczeństwo związku. Pojawił się jednak pewien problem, bowiem niemal wszyscy uczestnicy wykształcili przeciwciała co zmusza badaczy do zmienienia formuły.
Wzmacnianie Auto-fagocytozy (samooczyszczenia się komórki)
Choroba Parkinsona wiążę się także z akumulacją źle sformowanych protein i tworzeniu ciał Lewy’ego. Mówimy tu nie tylko o alfa-synukleinie, ale także o ubikwitynie, czyli białku, którego rolą jest naznaczanie innych białek przeznaczonych do komórkowej utylizacji. Ponadto ponad połowa (56%) zmagających się z ChP ma zmiany genetyczne organelli, charakterystyczne również dla choroby spichrzania lizosomanego (z ang. LSDs – lisosomal storage disease) W obu przypadkach, LSDs i ChP, problem polega na tym, że pewne organelle – lizosomy nie działają prawidłowo. Aby wyjaśnić zagadnienie przyrównajmy nasze komórki do średniej wielkości miasta, zaś lizosomy są w nim źle działającym odpowiednikiem miejskiej spalarni śmieci. Generuje to odpady, które stają się toksyczne dla naszego organizmu. Jedna z mutacji (mutacja GBA) odpowiedzialna za chorobę LSDs występuję także w 5-8 % chorych na Parkinsona. Pacjenci z tą odmianą ChP są statystycznie diagnozowani o 5 lat wcześniej i mają przy tym nasilone problemy z utrzymaniem prawidłowej postawy ciała, chodem oraz ulegają szybszemu osłabieniu funkcji poznawczych [6]. Niedawno ukazał się raport z badań klinicznych przeprowadzony na 20 uczestnikach przez firmę Val Andel z użyciem leku Ambroxol i pomimo, że była to mała próba lek okazał się być skuteczny w zmniejszeniu gromadzonej się alfa-synukleiny.
Ponadto Firma Pervail therapeutics (Pr001) postawiła na terapię genową, używając do tego szkieletu wirusa AAV, która ma pomóc dostarczyć lek do OUN. Oba te wydarzenia powinny zainteresować ludzi, u których zdiagnozowano chorobę Gauchera, bowiem cierpią oni z powodu tej samej mutacji.
Nilotinib – cABL inhibitor.
Lek stosowany w leczeniu białaczki, to kolejna substancja, która była testowana pod kątem ChP. Niestety obecnie zakończone badanie fazy drugiej NCT03205488, którego treściwy opis można znaleźć na stronie fundacji Michaela J Foxa, nie przyniosły zadowalających wyników.
LRRK2 inhibitor
Niektórzy cierpią na Parkinsona z powodu mutacji genu LRRK. W leczenie tej odmiany zaangażował się Sergey Brin, jeden z założycieli firmy Google, którego mama została zdiagnozowana z tą odmianą. Wydarzenie to było przyczyną, że Sergey Brin, jeden z najbogatszych ludzi w 2020, angażuje pokaźne sumy pieniędzy w znalezienie leku. Pacjenci z tą odmianą są diagnozowani wcześniej, mają łagodniejsze objawy motoryczne, ale za to nasiloną dystonię, czyli mimowolne wyginające i skręcające ruchy ciała oraz problemy ze snem. Firma Denali zakończyła fazę I test (DNL-201) i zgodnie z oświadczeniem prasowym z 19 maja 2020 wyselekcjonują oni jeden z prototypów do fazy drugiej.
GLP-1 agonista (wzmacniacz)
W badaniach przedklinicznych wywnioskowano, że GLP-1a, czyli antagonista glukagonopodobnego peptydu jelitowego-1, może przyczynić się do leczenia ChP poprzez obniżanie stresu oksydacyjnego. Innymi słowy ma on pomóc przywrócić zachwianą równowagę w funkcjonowaniu komórki na poziomie biochemicznym. W 2017 roku opublikowano wyniki Van Andel grupy, które stwierdzają, że w przypadku motoryki (część trzecia MDS-UPDRS) nastąpiła stabilizacja objawów. Prowadzi się szereg badań w fazie II i zgodnie z tym co powiedział dr Stott firmy farmaceutyczne przymierzają się do rozpoczęcia fazy trzeciej.
Wspomaganie mitochondriów
Oczywistym jest, że mitochondria, czyli ta cześć naszych komórek, gdzie produkuje się energię, z wiekiem słabną. Charakterystyczne jest, że u chorych na Parkinsona proces ten jest jeszcze bardziej nasilony.
Kwas ursodeoxycholowy (UDCA)
Jest to ten sam kwas, który w naszym woreczku żółciowym jest odpowiedzialny za degeneracje kamieni żółciowych okazał się hamować proces apoptozy (programowej śmierci komórki), która jest uaktywniana, gdy komórka jest uszkodzona bądź nie działa na odpowiednim poziomie. Wstępne badaniach okazały się na tyle obiecujące, że obecnie prowadzi się badania w fazie II, którym patronuje prof. Bandmann z uniwersytetu w Sheffield (Wlk. Brytania)
Rybozyd Nikotynoamidu
Jest to jedna z 3 forma witaminy B3 czyli: niacyny nicotynoamidy i rybozydu nikotynoamidy i ta ostatnia jest badana w aspekcie wzmacniania mitochondriów. Według publikacji z września 2020, pomimo długich dekad badań, dysponujemy jedynie poszlakowymi dowodami co do skuteczności terapii witaminą B3. Tym niemniej w konkluzji możemy przeczytać, że ponieważ część pacjentów wykazała poprawę stanu zdrowia, dalsze badania są jak najbardziej zasadne [7].
GDNF – Czynnik Neurotroficzny (pobudzające wzrost)
Pomimo nie do końca pozytywnych wyników prób klinicznych badacze wciąż widzą w tym potencjał [artykuł.ang.]. A ponieważ dr Stott tylko o tym wspomniał szczegóły tych nie całkiem udanych badań omówię w innym artykule. Tym niemniej wyniki są ciekawe i nie oznaczają one definitywnego końca badań nad GDNF.
Co Niesie Nam Przyszłość
Dr. Stutt puentując swoją prelekcję wspomniał o trzech aspektach związanych z ChP. Po pierwsze przyznał, że innowacje w dziedzinie badań Parkinsona zachodzą tak szybko, że nie zdziwi go, jeśli w ciągu kilku następnych lat zobaczymy znaczące zmiany w leczeniu tej przypadłości. Tak na przykład część badaczy sądzi, że w 21-szym wieku znajdą się wirusy mogące być wykorzystany jako środek transportu leku do OUN co sprawi, że zamiast wiercić dziurę w głowie pacjenta, lek będzie mógł być podawany dożylnie. Ponadto stwierdził, że czas patrzenia na chorobę Parkinsona jako jednolitą jednostkę chorobową dobiega końca, bowiem zaczyna się era kategoryzowania pacjentów na poszczególne podtypy. Innymi słowy pomimo, że chorobę diagnozuje się klinicznie na podstawie symptomów to co raz większą role w leczeniu zaczyna odgrywać przyczyna, czyli etiologia, bo od tego uzależniony jest dobór terapii. Trzeci wspomniany element odnosi się do stawianie większego nacisku na rozpoczęcie interwencji przed wystąpieniem pierwszych objawów. Dysponujemy już taką wiedzą, że należy zacząć myśleć o selekcjonowaniu tych ludzi, którzy z genetycznego punktu widzenia, mają predyspozycje do zachorowania. Dr Stott przestrzega nas jednak przed hura-optymizmem, twierdzi on nawet, że dla niego jako badacza szklanka nie jest nawet do połowy pełna, jest po prostu pusta.[1][2] I o ile jest to godna postawa ambitnego badacza, nasza jako pacjentów musi być nieco inna. Musimy bowiem pamiętać, że w świetle wszystkich znanych mi faktów, ze wszystkich chorób neurodegeneracyjnych, to choroba Parkinsona ma największe szanse na znalezienie panaceum. Co prawda nie będzie to jutro, może nawet nie w przyszłym roku, ale jestem przekonany, że ten dzień nadejdzie a do tego czasu racjonalny optymizm powinien nam codziennie towarzyszyć, motywując tym samym do podjęcia codziennych zmagań nawet jeżeli głaz ponownie stoczy się na dno wąwozu.
Ważna postać w świecie transplantacji komórek macierzystych (wróć)
Główną funkcją skorupy jest regulowanie ruchów zarówno w stadium planowania jak i ich egzekucji. (wróć)
[3] Tabelka z opisem faz badań klinicznych jest dostępny pod tym linkiem.
Bibliografia
| [1] | Zella S. M. Metzdorf J. Ciftci E. et.al., “Emerging immunotherapies for Parkinson disease,” Neurology and therapy, vol. 8, no. 1, pp. 29-44, 2019. |
| [2] | West C. L. Mao Y. K. Delungahawatta T. et. al., “Squalamine Restores the Function of the Enteric Nervous System in Mouse Models of Parkinson’s Disease.,” Journal of Parkinson’s Disease,, pp. (Preprint 1-15), 2020. |
| [3] | Hauser R. A. Sutherland D. Madrid J. A. et.al., “Targeting neurons in the gastrointestinal tract to treat Parkinson’s disease,” Clinical Parkinsonism & Related Disorders, vol. 1, pp. 2-7, 2019. |
| [4] | B. R. F. S. e. Limbocker R. Mannini, “Limbocker, R., Mannini, B., Ruggeri, F. S., Cascella, R., Xu, C. K., Perni, M., … & Kreiser, R. P. (2020). Trodusquemine displaces protein misfolded oligomers from cell membranes and abrogates their cytotoxicity through a generic mechanism.,” Communications biology, vol. 3, no. 1, pp. 1-10, 2020. |
| [5] | Racette B. A. Gross A. Vouri S. M. et. al.., “Immunosuppressants and risk of Parkinson disease,” Annals of clinical and translational neurology, vol. 5, no. 7, pp. 870-875, 2018. |
| [6] | T. C. P. Trust, “The Ambroxol Trial – The facts,” The Cure Parkinson’s Trust, [Online]. Available: https://www.cureparkinsons.org.uk/ambroxol-the-facts. [Accessed 30 12 2020]. |
| [7] | Radenkovic D. & Verdin E., “Clinical Evidence for Targeting NAD Therapeutically.,” Pharmaceuticals,, vol. 13, no. 9, p. 247, 2020. |